Moléculas 3d de sales químicas
- Plata I
- Mercurio
- Estroncio
- Plata II
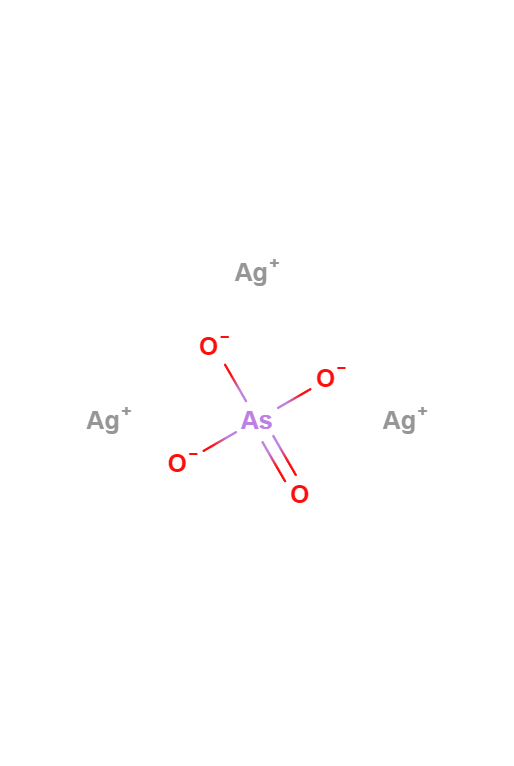
Arseniato de Plata
El Arseniato de Plata es un compuesto inorgánico con la fórmula Ag3AsO4. Se ha utilizado en análisis cualitativos para distinguir entre fosfato y soluciones de arseniato.
Arseniato de Plata
 Enlace simple
Enlace simple
Enlace doble
 Enlace Triple
Enlace Triple
Enlace cuña

Enlace hash
Bromuro de Mercurio (I)
El Bromuro de Mercurio (I) es un compuesto químico de fórmula química es Hg2Br2. Cambia de color de blanco a amarillo cuando se calienta y se hace fluorescente en color salmón cuando se expone a la luz ultravioleta. Tiene aplicaciones en dispositivos acústico-ópticos.
Bromuro de Mercurio
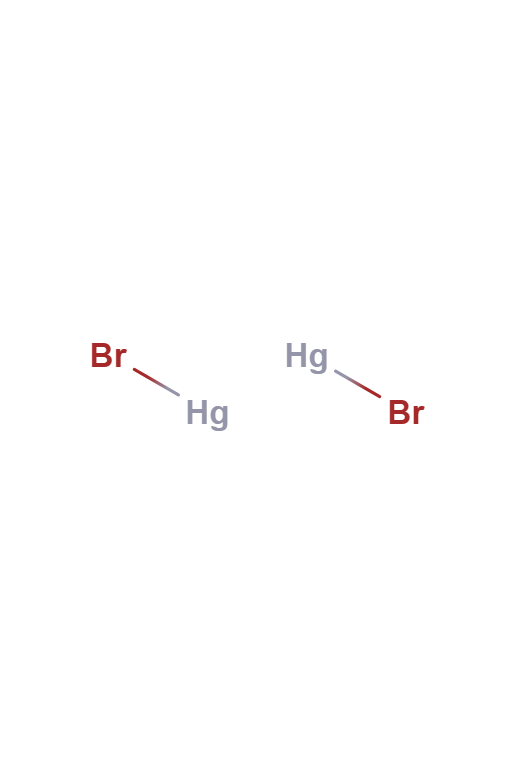
 Enlace simple
Enlace simple
Enlace doble
 Enlace Triple
Enlace Triple
Enlace cuña

Enlace hash
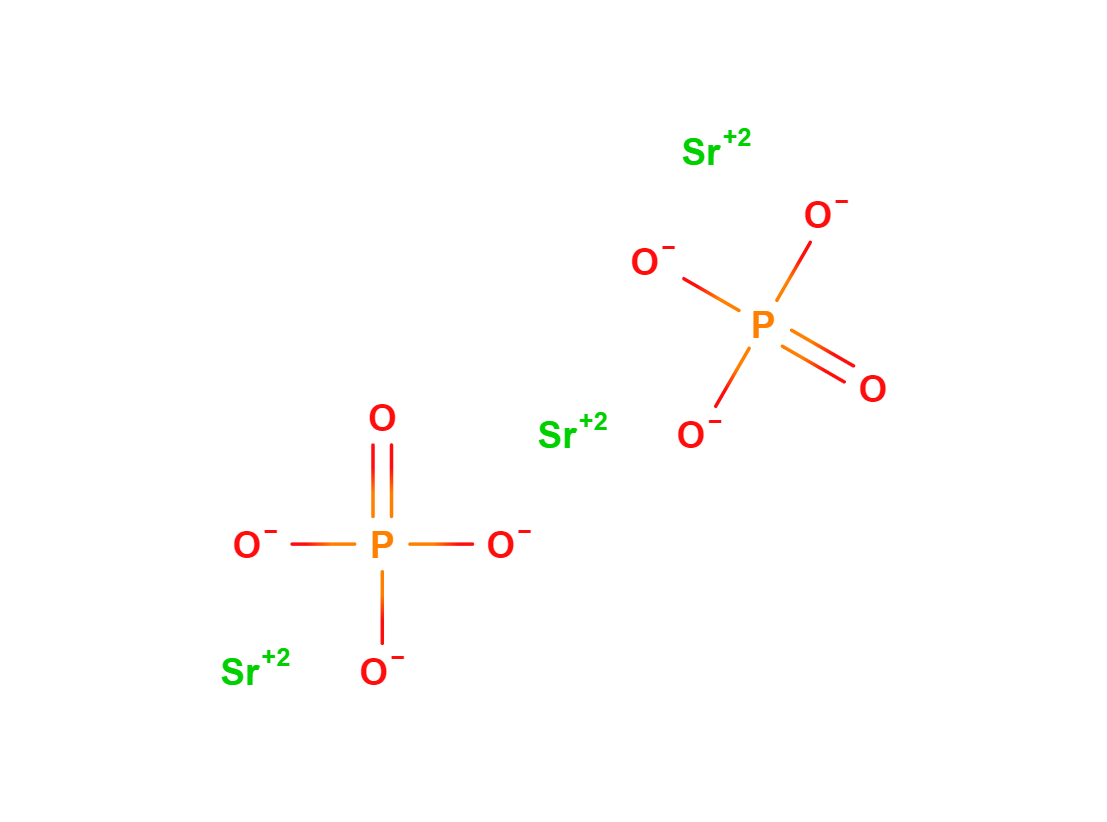
Fosfato de Estroncio
El Fosfato de Estroncio es un compuesto químico de formula O8P2Sr3. Es una substancia cristalina usada en medicina y en la industria.
Fosfato de Estroncio
 Enlace simple
Enlace simple
Enlace doble
 Enlace Triple
Enlace Triple
Enlace cuña

Enlace hash
Gigantes de la ciencia
«Si he visto más lejos es porque estoy a hombros de gigantes»
Isaac Newton

Antoine-Laurent de Lavoisier
–

Marie Curie
–
Hazte gigante
Tu camino para ser un gigante del conocimiento comienza con estos cursos gratuitos de primer nivel


Sales: reacciones químicas y aplicaciones



Reacciones redox en la industria y la naturaleza



Reacciones de oxidación-reducción: conceptos básicos



Ácidos y bases: reacciones químicas y aplicaciones



Reacciones Químicas y Cálculos Estequiométricos



Formulación y nomenclatura de compuestos químicos



El Enlace Químico y las Interacciones Moleculares

Desarrollo profesional docente
Programas de formación orientados a fortalecer la práctica educativa en ciencias y tecnología


Teaching Computational Thinking



HP Digital Skills for Educators – Google Workspace



BlendedX: Blended Learning with edX



Higher education assessing in the age of AI